En elektrisk strömkälla är en anordning som genererar elektrisk ström i en sluten krets. Hittills har många olika typer av källor uppfunnits. Varje typ används för ett specifikt ändamål.
Innehållet i .
Typer av elektriska strömkällor
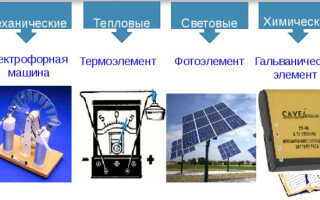
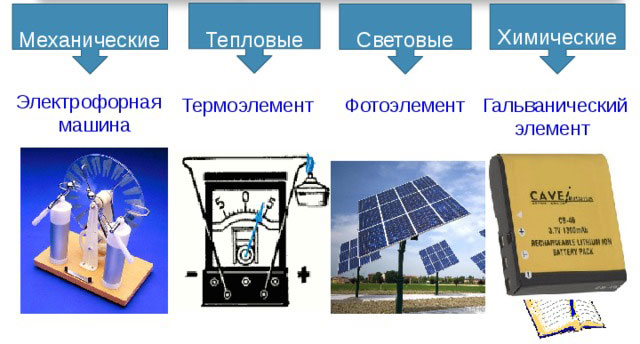
Det finns följande typer av elektriska strömkällor:
- mekanisk;
- termisk;
- ljus;
- kemikalier.
Mekaniska källor
Dessa källor omvandlar mekanisk energi till elektrisk energi. Omvandlingen sker i särskilda anordningar - generatorer. De viktigaste generatorerna är turbogeneratorer, där den elektriska maskinen drivs av en gas- eller ångström, och vattenkraftgeneratorer, som omvandlar energin från fallande vatten till elektricitet. Det är de mekaniska omvandlarna som producerar den mesta elen på jorden.

Termiska källor
Här omvandlas värmeenergi till elektricitet. Den elektriska strömmen genereras av temperaturskillnaden mellan två par metaller eller halvledare som är i kontakt med varandra - termoelement. I detta fall transporteras laddade partiklar från den uppvärmda sektionen till den kalla sektionen. Storleken på strömmen beror direkt på temperaturskillnaden: ju större skillnaden är, desto större är den elektriska strömmen. Termokopplar som är baserade på halvledare ger en värmeeffekt som är 1000 gånger större än bimetalltermokopplar, vilket gör att de kan användas för att skapa strömkällor. Termokopplar av metall används endast för att mäta temperatur.

TIP! För att göra en termokoppling måste två olika metaller sammanfogas.
Nya grundämnen har nu utvecklats genom omvandling av den värme som genereras av det naturliga sönderfallet av radioaktiva isotoper. Sådana element kallas radioisotopiska termoelektriska generatorer. En väl beprövad generator i rymdfarkoster använder isotopen plutonium-238. Den ger en effekt på 470 W vid en spänning på 30 V. Eftersom halveringstiden för denna isotop är 87,7 år är generatorns livslängd mycket lång. En bimetallisk termokoppling fungerar som en omvandlare från värme till elektricitet.
Ljuskällor
Med utvecklingen av halvledarfysiken i slutet av 1900-talet dök nya strömkällor upp - solceller, där ljusenergi omvandlas till elektrisk energi. De utnyttjar halvledarnas egenskap att producera spänning när de utsätts för ljus. Särskilt kiselhalvledare har denna effekt. Effektiviteten hos sådana celler överstiger dock inte 15 %. Solceller har blivit oumbärliga inom rymdindustrin och har även börjat användas i vardagen. Priset på sådana kraftkällor sjunker ständigt, men är fortfarande ganska högt: cirka 100 rubel per 1 watt effekt.

Kemiska nätaggregat
Alla kemiska energikällor kan delas in i tre grupper:
- Galvanisk
- Batterier
- Termisk
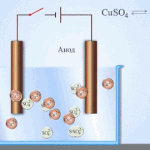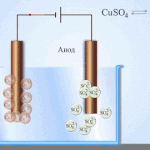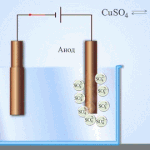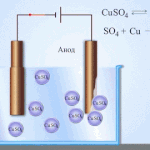
Galvaniska celler fungerar genom interaktion mellan två olika metaller som placeras i en elektrolyt. Metallerna och elektrolytparen kan vara olika kemiska element och deras föreningar. Elementets typ och egenskaper beror på detta.
VIKTIGT! Galvaniska celler används bara en gång, dvs. de kan inte återskapas när de väl är urladdade.
Det finns tre typer av galvaniska celler (eller batterier):
- Saltlösning;
- Alkalisk;
- Litium.
Salt- eller torrbatterier använder en pastaliknande elektrolyt som tillverkas av ett salt av någon metall och som placeras i en zinkbägare. Katoden är en mangangrafitstav som placeras i bägaren. De billiga materialen och den enkla tillverkningen gjorde dessa batterier till de billigaste av alla. De är dock klart sämre än alkaliska och litiumbatterier.

Alkaliska batterier använder en pastaliknande alkalisk lösning av kaliumhydroxid som elektrolyt. Zinkanoden har ersatts av zinkpulver, vilket har ökat cellens strömstyrka och drifttid. Dessa celler håller upp till 1,5 gånger längre än saltceller.
I litiumcellen består anoden av litium, en alkalimetall, vilket har ökat drifttiden avsevärt. Men samtidigt har priset ökat på grund av den relativt höga kostnaden för litium. Dessutom kan litiumbatterier ha olika spänningar beroende på katodmaterialet. Batterier finns tillgängliga med spänningar från 1,5 V till 3,7 V.
Batterier är elektriska strömkällor som kan utsättas för många laddnings- och urladdningscykler. De viktigaste typerna av batterier är:
- Bly-syra;
- Litiumjon;
- Nickel-kadmium.
Blybatterier består av blyplattor som är nedsänkta i en svavelsyralösning. När en extern elektrisk krets är sluten sker en kemisk reaktion som omvandlar bly till blysulfat vid katoden och anoden och vatten bildas. Under laddningsprocessen reduceras blysulfat vid anoden till bly och blydioxid vid katoden.

BAKGRUND! En enda bly-zinkbattericell ger en spänning på 2 V. Genom att koppla cellerna i serie är det möjligt att få en spänning som är multipel av 2. I bilbatterier är spänningen t.ex. 12 V, eftersom 6 celler är anslutna.
Litiumjonbatteriet har fått sitt namn från det faktum att elektrolytens bärare av elektricitet är litiumjoner. Jonerna skapas på en katod som består av litiumsalt på ett substrat av aluminiumfolie. Anoden består av olika material: grafit, koboltoxider och andra föreningar på ett substrat av kopparfolie.
Spänningen kan vara mellan 3 V och 4,2 V, beroende på vilka komponenter som används. På grund av deras låga självavladdning och höga antal laddnings- och urladdningscykler har litiumjonbatterier blivit mycket populära i hushållsapparater.
VIKTIGT! Litiumjonbatterier är mycket känsliga för överladdning. För att ladda dem ska du därför endast använda laddare som är avsedda för dem och som har särskilda kretsar inbyggda för att förhindra överladdning. Annars kan batteriet sönderfalla och börja brinna.

Nickel-kadmiumbatterier har en katod av nickelsalt på ett stålgaller, en anod av kadmiumsalt på ett stålgaller och elektrolyten är en blandning av litiumhydroxid och kaliumhydroxid. Den nominella spänningen för ett sådant batteri är 1,37 V. Batteriet kan laddas och laddas ur mellan 100 och 900 cykler.
TIP! Ni-Cd-batterier kan lagras i urladdat tillstånd, till skillnad från litiumjonbatterier.
Termiska kemiska celler fungerar som reservkraftkällor. De ger utmärkt strömtäthet men har en kort livslängd (upp till en timme). De används främst inom rakettekniken där tillförlitlighet och kort livslängd krävs.
VIKTIGT! Till en början kan termiska kemiska källor inte leverera elektrisk ström. De innehåller elektrolyt i fast form och måste värmas till 500-600 °C för att fungera. Uppvärmningen sker med hjälp av en speciell pyroteknisk blandning som antänds i rätt ögonblick.
Skillnaden mellan en verklig och en idealisk källa
En idealisk källa måste enligt fysikens lagar ha ett oändligt inre motstånd för att säkerställa att den elektriska strömmen i belastningen är konstant. Reella källor har ett ändligt inre motstånd, vilket innebär att strömmen beror på både den externa belastningen och det inre motståndet.
Detta är i korthet allt som finns att säga om de olika strömkällor som finns tillgängliga i dag. Som framgår av översikten har det idag skapats ett imponerande antal källor med egenskaper som lämpar sig för alla tillämpningar.
Relaterade artiklar: