On usein ongelmallista päättää, kumpi elektrodi on katodi ja kumpi anodi. Hyvä alku on päästä yhteisymmärrykseen termeistä.
Sisältö
Katodin ja anodin käsite - yksinkertainen selitys
Monimutkaisissa aineissa yhdisteiden atomien väliset elektronit eivät ole jakautuneet tasaisesti. Vuorovaikutus aiheuttaa hiukkasten siirtymisen yhden aineen atomista toisen aineen atomiin. Reaktiota kutsutaan hapettumis-pelkistymisreaktioksi. Elektronien menetystä kutsutaan hapettumiseksi, ja elektronit luovuttavaa ainetta kutsutaan pelkistäväksi aineeksi.
Elektronien lisäämistä kutsutaan pelkistymiseksi, ja elektronit vastaanottava alkuaine on hapetin. Elektronien siirto pelkistävästä aineesta hapettavaan aineeseen voi tapahtua ulkoisen virtapiirin kautta, jolloin sitä voidaan käyttää sähköenergian lähteenä. Laitteita, jotka muuttavat kemiallisen reaktion energian sähköenergiaksi, kutsutaan galvaanisiksi kennoiksi.
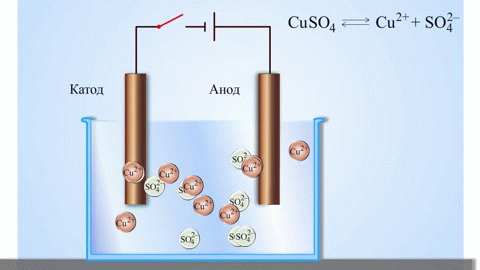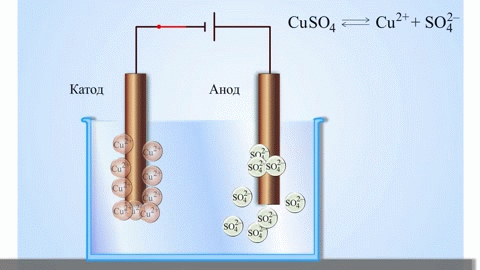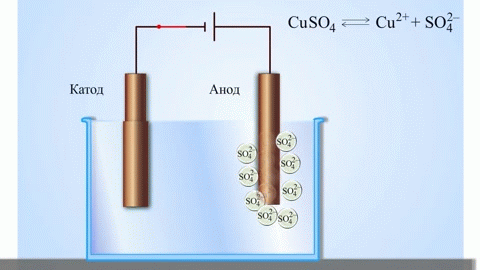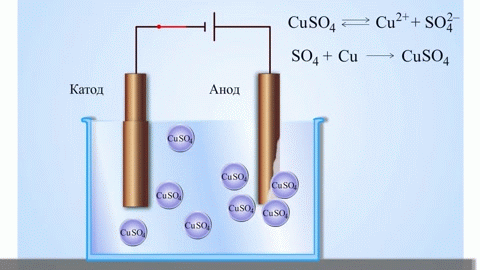
Yksinkertaisin klassinen esimerkki galvaanisesta kennosta on kaksi eri metalleista valmistettua levyä, jotka on upotettu elektrolyyttiliuokseen. Tässä järjestelmässä hapettuminen tapahtuu yhdessä metallissa ja pelkistyminen toisessa.
TÄRKEÄÄ! Elektrodia, jossa hapettuminen tapahtuu, kutsutaan anodiksi. Elektrodia, jossa pelkistyminen tapahtuu, kutsutaan katodiksi.
Kupari-sinkki-galvaaninen kenno, joka toimii absorboimalla sinkin ja kuparisulfaatin välisen reaktion energiaa, on tuttu esimerkki koulujen kemian oppikirjoista. Jacoby-Daniel-laitteessa kuparilevy asetetaan kuparisulfaattiliuokseen (kuparielektrodi) ja sinkkilevy upotetaan sinkkisulfaattiliuokseen (sinkkielektrodi). Sinkkielektrodi luovuttaa kationeja liuokseen, jolloin liuokseen muodostuu ylimääräinen positiivinen varaus, kun taas kuparielektrodin kohdalla liuoksesta poistuu kationeja, jolloin liuos on negatiivisesti varautunut.
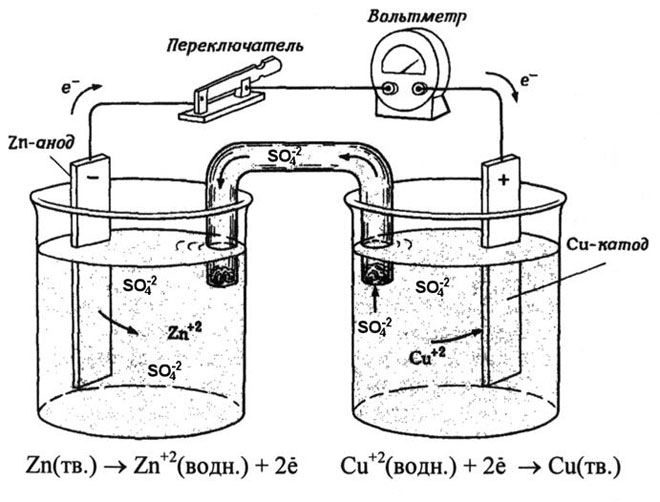
Ulkoisen virtapiirin sulkeminen saa elektronit virtaamaan sinkkielektrodista kuparielektrodiin. Tasapainosuhteet faasien rajoilla katkeavat. Tapahtuu redox-reaktio.
Spontaanin kemiallisen reaktion energia muunnetaan sähköenergiaksi.
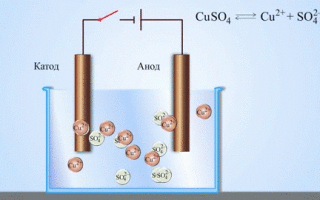
Jos kemiallinen reaktio käynnistetään ulkoisella sähköenergialla, syntyy prosessi, jota kutsutaan elektrolyysiksi. Elektrolyysin aikana tapahtuvat prosessit ovat päinvastaisia kuin galvaanisen kennon aikana tapahtuvat prosessit.
HUOMIO! Elektrodia, jolla pelkistyminen tapahtuu, kutsutaan myös katodiksi, mutta elektrolyysissä se on negatiivisesti varautunut ja anodi on positiivisesti varautunut.
Sähkökemialliset sovellukset
Anodit ja katodit osallistuvat moniin kemiallisiin reaktioihin:
- Elektrolyysi;
- Sähköinen uuttaminen;
- Galvanointi;
- Galvanointi.
Sulan yhdisteiden ja vesiliuosten elektrolyysillä tuotetaan metalleja, puhdistetaan metalleja epäpuhtauksista ja uutetaan arvokkaita komponentteja (elektrolyyttinen jalostus). Levyt valetaan jalostettavasta metallista. Levyt sijoitetaan anodeiksi elektrolyyseriin. Metalli liuotetaan sähkövirran avulla. Sen kationit siirtyvät liuokseen ja purkautuvat katodilla muodostaen puhtaan metallin saostuman. Alkuperäisen raakametallilevyn sisältämät epäpuhtaudet joko jäävät liukenemattomiksi anodilietteeksi tai siirtyvät elektrolyyttiin, jossa ne poistetaan. Kupari, nikkeli, lyijy, kulta, hopea ja tina jalostetaan elektrolyyttisesti.
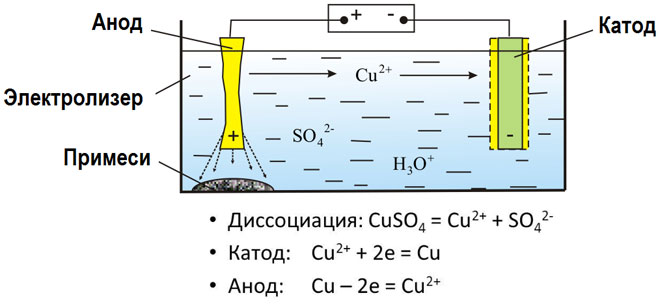
Elektrouuttaminen on prosessi, jossa metalli uutetaan liuoksesta elektrolyysin aikana. Jotta metalli siirtyisi liuokseen, se käsitellään erityisreagensseilla. Prosessissa erotetaan erittäin puhdasta metallia katodilla. Näin tuotetaan sinkkiä, kuparia ja kadmiumia.
Korroosion välttämiseksi, tuotteen lujittamiseksi ja koristeellisuuden lisäämiseksi yhden metallin pinta pinnoitetaan toisella metallilla. Tämä prosessi tunnetaan nimellä galvanointi.

Sähkömuovaus on prosessi, jossa kolmiulotteisista esineistä valmistetaan metallikopioita metallin sähköpinnoituksella.

Tyhjiöelektroniikan sovellukset
Tyhjiölaitteen katodin ja anodin periaatetta voidaan havainnollistaa elektroniputken avulla. Se näyttää ilmatiiviisti suljetulta säiliöltä, jonka sisällä on metalliosia. Laitetta käytetään sähköisten signaalien tasasuuntaamiseen, tuottamiseen ja muuntamiseen. Erotus tehdään elektrodien lukumäärän mukaan:
- diodit;
- triodit;
- tetrodit;
- pentodit jne.
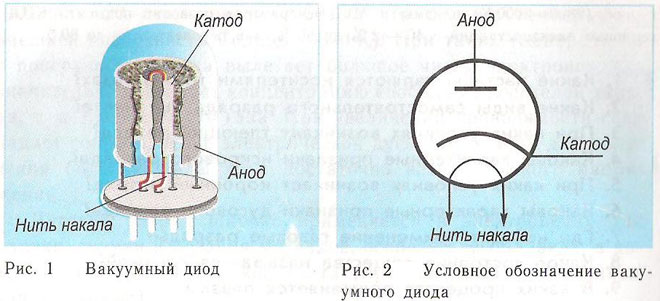
Diodi on tyhjiölaite, jossa on kaksi elektrodia, katodi ja anodi. Katodi kytketään virtalähteen negatiiviseen napaan ja anodi positiiviseen napaan. Katodin tehtävänä on emittoida elektroneja, kun se kuumennetaan sähkövirralla tiettyyn lämpötilaan. Elektronien avulla katodin ja anodin välille muodostuu avaruusvaraus. Nopeimmat elektronit ryntäävät kohti anodia ja ohittavat avaruusvarauksen negatiivisen potentiaaliesteen. Anodi vastaanottaa hiukkaset. Ulkoiseen virtapiiriin syntyy anodinen virta. Elektronien virtausta ohjataan lisäelektrodeilla, joihin syötetään sähköinen potentiaali. Diodeja käytetään vaihtovirran muuntamiseen tasavirraksi.
Elektroniikan sovellukset
Nykyään käytetään puolijohdediodityyppejä.
Elektroniikassa käytetään laajalti diodien ominaisuutta kulkea virtaa eteenpäin ja olla kulkematta virtaa taaksepäin.
LEDin toiminta perustuu puolijohdekiteiden ominaisuuteen hehkua, kun p-n-liitoksen läpi kulkee virta eteenpäin.
Galvaaniset tasavirtalähteet - akut
Kemiallisia sähkövirtalähteitä, joissa tapahtuu palautuvia reaktioita, kutsutaan ladattaviksi akuiksi: ne ladataan uudelleen ja käytetään toistuvasti.

Kun lyijyakku toimii, tapahtuu redox-reaktio. Metallinen lyijy hapettuu ja luopuu elektroneistaan, jolloin elektronit vastaanottava lyijydioksidi pelkistyy. Akun metallinen lyijy on anodi, ja se on negatiivisesti varautunut. Lyijydioksidi on katodi ja positiivisesti varautunut.
Akun purkautuessa katodin ja anodin aineet ja niiden elektrolyytti, rikkihappo, kuluvat. Akun lataamiseksi se kytketään virtalähteeseen (plus plussaan, miinus miinukseen). Virran suunta on nyt päinvastainen kuin akun purkautuessa. Elektrokemialliset prosessit elektrodeissa ovat "käänteisiä". Lyijyelektrodista tulee nyt katodi, jossa tapahtuu pelkistymisprosessi, ja lyijydioksidista tulee anodi, jossa tapahtuu hapettumisprosessi. Akun tarvitsemat aineet syntyvät jälleen akussa.
Miksi tämä on hämmentävää?
Ongelma johtuu siitä, että tiettyä varauksen merkkiä ei voida kiinnittää kiinteästi anodiin eikä katodiin. Usein katodi on positiivisesti varautunut elektrodi ja anodi on negatiivinen elektrodi. Usein, mutta ei aina. Kaikki riippuu elektrodissa tapahtuvasta prosessista.
VAROITUS! Elektrolyyttiin sijoitettu osa voi olla sekä anodi että katodi. Kaikki riippuu prosessin tarkoituksesta: toisen metallikerroksen levittäminen tai metallikerroksen poistaminen.
Anodin ja katodin tunnistaminen
Sähkökemiassa anodi on elektrodi, jossa tapahtuu hapettuminen, ja katodi on elektrodi, jossa tapahtuu pelkistyminen.
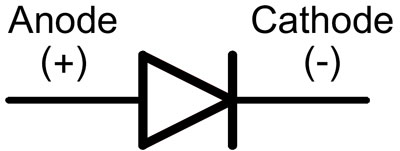
Diodissa johtimia kutsutaan anodiksi ja katodiksi. Virta kulkee diodin läpi, jos anodijohto on kytketty plussaan ja katodijohto miinukseen.
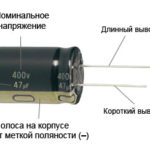
Uuden ledin, jossa on leikkaamattomat nastat, anodi ja katodi määritetään silmämääräisesti pituuden perusteella. Katodi on lyhyempi.

Jos koskettimet ovat katkenneet, niihin kiinnitetty paristo auttaa. Valo näkyy, kun polariteetit vastaavat toisiaan.
Anodin ja katodin merkki
Sähkökemiassa on oikeampaa puhua elektrodeissa tapahtuvista prosesseista kuin elektrodien merkeistä. Pelkistysreaktio tapahtuu katodilla ja hapetusreaktio anodilla.
Sähkötekniikassa katodi kytketään virtalähteen negatiiviseen napaan ja anodi positiiviseen napaan.
Aiheeseen liittyvät artikkelit: