மின்னோட்ட மூலமானது ஒரு மூடிய சுற்றுவட்டத்தில் மின்சாரத்தை உருவாக்கும் ஒரு சாதனமாகும். இப்போதெல்லாம், அத்தகைய ஆதாரங்களின் ஏராளமான வகைகள் கண்டுபிடிக்கப்பட்டுள்ளன. ஒவ்வொரு வகையும் ஒரு குறிப்பிட்ட நோக்கத்திற்காக பயன்படுத்தப்படுகிறது.
உள்ளடக்கம் .
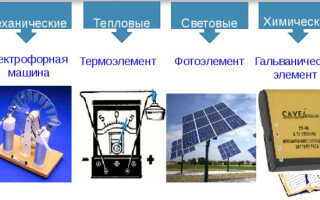
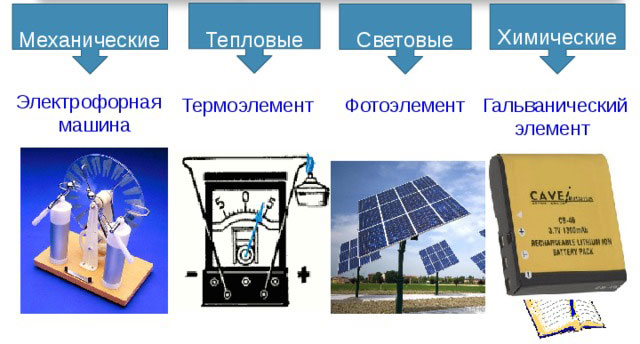
மின்சார ஆதாரங்களின் வகைகள்
பின்வரும் வகையான மின்சார ஆதாரங்கள் உள்ளன:
- இயந்திரவியல்;
- வெப்ப;
- ஒளி;
- இரசாயன.
இயந்திர ஆதாரங்கள்
இந்த ஆதாரங்களில், இயந்திர ஆற்றல் மின் ஆற்றலாக மாற்றப்படுகிறது. மாற்றம் சிறப்பு சாதனங்களில் மேற்கொள்ளப்படுகிறது - ஜெனரேட்டர்கள். முக்கிய ஜெனரேட்டர்கள் டர்பைன் ஜெனரேட்டர்கள் ஆகும், அங்கு ஒரு மின்சார இயந்திரம் வாயு அல்லது நீராவி ஓட்டத்தால் இயக்கப்படுகிறது, மற்றும் நீர் ஜெனரேட்டர்கள், விழும் நீரின் ஆற்றலை மின்சாரமாக மாற்றும். பூமியில் பெரும்பாலான மின்சாரத்தை உற்பத்தி செய்யும் இயந்திர மாற்றிகள் ஆகும்.

வெப்ப ஆதாரங்கள்
இங்குதான் வெப்ப ஆற்றல் மின்சாரமாக மாற்றப்படுகிறது. இரண்டு ஜோடி தொடர்பு உலோகங்கள் அல்லது குறைக்கடத்திகள் - தெர்மோகப்பிள்களுக்கு இடையிலான வெப்பநிலை வேறுபாட்டால் மின்சாரம் உருவாக்கப்படுகிறது. இந்த வழக்கில், சார்ஜ் செய்யப்பட்ட துகள்கள் சூடான பகுதியிலிருந்து குளிர்ந்த பகுதிக்கு கொண்டு செல்லப்படுகின்றன. மின்னோட்டத்தின் அளவு நேரடியாக வெப்பநிலை வேறுபாட்டைப் பொறுத்தது: அதிக வேறுபாடு, அதிக மின்சாரம்.செமிகண்டக்டர்களை அடிப்படையாகக் கொண்ட தெர்மோகப்பிள்கள் பைமெட்டல் தெர்மோகப்பிள்களை விட 1000 மடங்கு அதிகமான வெப்ப வெளியீடுகளைக் கொடுக்கின்றன, எனவே அவை தற்போதைய மூலங்களை உருவாக்கப் பயன்படுத்தப்படலாம். உலோக தெர்மோகப்பிள்கள் வெப்பநிலையை அளவிட மட்டுமே பயன்படுத்தப்படுகின்றன.

உதவிக்குறிப்பு! ஒரு தெர்மோகப்பிள் செய்ய, 2 வெவ்வேறு உலோகங்கள் ஒன்றாக இணைக்கப்பட வேண்டும்.
கதிரியக்க ஐசோடோப்புகளின் இயற்கையான சிதைவால் வெளியிடப்படும் வெப்பத்தின் மாற்றத்தின் அடிப்படையில் புதிய தனிமங்கள் இப்போது உருவாக்கப்பட்டுள்ளன. இத்தகைய தனிமங்கள் ரேடியோஐசோடோப் தெர்மோஎலக்ட்ரிக் ஜெனரேட்டர் என்று அழைக்கப்படுகின்றன. விண்கலத்தில் புளூட்டோனியம்-238 ஐசோடோப்பு பயன்படுத்தப்படும் நன்கு நிரூபிக்கப்பட்ட ஜெனரேட்டர். இது 30 V மின்னழுத்தத்தில் 470 W இன் ஆற்றலை அளிக்கிறது. இந்த ஐசோடோப்பின் அரை ஆயுள் 87.7 ஆண்டுகள் என்பதால், ஜெனரேட்டரின் ஆயுட்காலம் மிக நீண்டது. ஒரு பைமெட்டாலிக் தெர்மோகப்பிள் ஒரு வெப்ப-மின்சார மாற்றியாக செயல்படுகிறது.
ஒளி மூலங்கள்
இருபதாம் நூற்றாண்டின் பிற்பகுதியில் குறைக்கடத்தி இயற்பியலின் வளர்ச்சியுடன் மின்னோட்டத்தின் புதிய ஆதாரங்கள் இருந்தன - சூரிய மின்கலங்கள், இதில் ஒளியின் ஆற்றல் மின் ஆற்றலாக மாற்றப்படுகிறது. ஒளி பாய்ச்சலுக்கு வெளிப்படும் போது மின்னழுத்தத்தை உருவாக்க அவை குறைக்கடத்திகளின் பண்புகளைப் பயன்படுத்துகின்றன. இந்த விளைவு சிலிக்கான் குறைக்கடத்திகளில் குறிப்பாக வலுவானது. இன்னும், அத்தகைய கலங்களின் செயல்திறன் 15% ஐ விட அதிகமாக இல்லை. சூரிய மின்கலங்கள் விண்வெளித் துறையில் இன்றியமையாததாகிவிட்டன மற்றும் அன்றாட வாழ்க்கையிலும் பயன்படுத்தத் தொடங்கியுள்ளன. அத்தகைய மின்சக்தி ஆதாரங்களின் விலை தொடர்ந்து குறைந்து வருகிறது, ஆனால் அது மிகவும் அதிகமாக உள்ளது: 1 வாட் சக்திக்கு சுமார் 100 ரூபிள்.

இரசாயன ஆதாரங்கள்
அனைத்து இரசாயன மூலங்களையும் 3 குழுக்களாகப் பிரிக்கலாம்:
- கால்வனிக்
- திரட்டிகள்
- வெப்ப
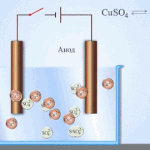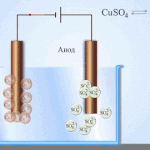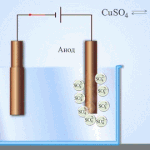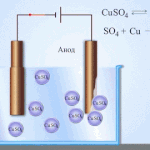
கால்வனிக் செல்கள் எலக்ட்ரோலைட்டில் வைக்கப்பட்டுள்ள இரண்டு வெவ்வேறு உலோகங்களின் தொடர்புகளின் அடிப்படையில் செயல்படுகின்றன. உலோகம் மற்றும் எலக்ட்ரோலைட் ஜோடிகள் வெவ்வேறு வேதியியல் கூறுகள் மற்றும் அவற்றின் சேர்மங்களாக இருக்கலாம். தனிமத்தின் வகை மற்றும் பண்புகள் இதைப் பொறுத்தது.
முக்கியமான! கால்வனிக் செல்கள் ஒரு முறை மட்டுமே பயன்படுத்தப்படுகின்றன, அதாவது ஒருமுறை வெளியேற்றப்பட்டால், அவற்றை மீட்டெடுக்க முடியாது.
கால்வனிக் மூலங்களில் 3 வகைகள் உள்ளன (அல்லது பேட்டரிகள்):
- உப்பு
- அல்கலைன்;
- லித்தியம்.
உப்பு அல்லது இல்லையெனில் "உலர்ந்த" பேட்டரிகள் ஒரு துத்தநாக கோப்பையில் வைக்கப்படும் சில உலோகத்தின் உப்பின் பேஸ்டி எலக்ட்ரோலைட்டைப் பயன்படுத்துகின்றன. கத்தோட் என்பது கோப்பையின் மையத்தில் உள்ள ஒரு கிராஃபைட்-மாங்கனீசு கம்பி ஆகும். மலிவான பொருட்கள் மற்றும் அத்தகைய பேட்டரிகளின் உற்பத்தியின் எளிமை ஆகியவை அவற்றை எல்லாவற்றிலும் மலிவானதாக ஆக்கியது. ஆனால் அவற்றின் குணாதிசயங்கள் அல்கலைன் மற்றும் லித்தியம் பேட்டரிகளை விட மிகவும் தாழ்வானவை.

அல்கலைன் பேட்டரிகள் கார பொட்டாசியம் ஹைட்ராக்சைட்டின் பேஸ்டிக் கரைசலை எலக்ட்ரோலைட்டாகப் பயன்படுத்துகின்றன. துத்தநாக அனோட் தூள் துத்தநாகத்தால் மாற்றப்பட்டது, இது கலத்தின் தற்போதைய வெளியீட்டையும் இயக்க நேரத்தையும் அதிகரித்தது. இந்த செல்கள் உப்பு செல்களை விட 1.5 மடங்கு நீண்ட காலம் நீடிக்கும்.
லித்தியம் கலத்தில், அனோட் லித்தியத்தால் ஆனது, ஒரு கார உலோகம், இது இயக்க நேரத்தை கணிசமாக அதிகரித்தது. ஆனால் அதே நேரத்தில், லித்தியத்தின் ஒப்பீட்டளவில் அதிக விலை காரணமாக விலை அதிகரித்துள்ளது. கூடுதலாக, லித்தியம் பேட்டரிகள் கேத்தோடின் பொருளைப் பொறுத்து வெவ்வேறு மின்னழுத்தங்களைக் கொண்டிருக்கலாம். 1.5V முதல் 3.7V வரையிலான மின்னழுத்தத்துடன் பேட்டரிகள் கிடைக்கின்றன.
பேட்டரிகள் - மின்னோட்டத்தின் ஆதாரங்கள், இது பல சார்ஜ்-டிஸ்சார்ஜ் சுழற்சிகளுக்கு உட்படுத்தப்படலாம். பேட்டரிகளின் முக்கிய வகைகள்:
- ஈய அமிலம்;
- லித்தியம்-அயன்;
- நிக்கல்-காட்மியம்.
லீட்-அமில பேட்டரிகள் சல்பூரிக் அமிலக் கரைசலில் மூழ்கியிருக்கும் ஈயத் தட்டுகளைக் கொண்டிருக்கும். வெளிப்புற மின்சுற்று மூடப்படும் போது, ஒரு இரசாயன எதிர்வினை ஏற்படுகிறது, இது கேத்தோடு மற்றும் அனோடில் ஈயத்தை ஈய சல்பேட்டாக மாற்றுகிறது, மேலும் நீர் உருவாகிறது. சார்ஜிங் செயல்பாட்டின் போது, அனோடில் ஈய சல்பேட் ஈயமாகவும், கேத்தோடில் ஈய டையாக்சைடாகவும் குறைக்கப்படுகிறது.

ஆதாரம்! ஒரு முன்னணி-துத்தநாக பேட்டரி செல் 2 V மின்னழுத்தத்தை உருவாக்குகிறது. செல்களை தொடரில் இணைப்பதன் மூலம், நீங்கள் எந்த மின்னழுத்தத்தையும் 2-ஐப் பெறலாம். எடுத்துக்காட்டாக, கார் பேட்டரிகளில், 6 செல்கள் இணைக்கப்பட்டுள்ளதால், மின்னழுத்தம் 12 V ஆகும்.
எலக்ட்ரோலைட்டில் உள்ள மின்சாரத்தின் கேரியர் லித்தியம் அயனிகள் என்பதால் லித்தியம்-அயன் பேட்டரி அதன் பெயரைப் பெற்றது. அயனிகள் கேத்தோடில் எழுகின்றன, இது அலுமினியத் தாளின் அடி மூலக்கூறில் லித்தியம் உப்பால் ஆனது. அனோட் வெவ்வேறு பொருட்களால் ஆனது: கிராஃபைட், கோபால்ட் ஆக்சைடுகள் மற்றும் செப்புப் படலத்தின் அடி மூலக்கூறில் உள்ள பிற கலவைகள்.
பயன்படுத்தப்படும் கூறுகளைப் பொறுத்து மின்னழுத்தம் 3 V மற்றும் 4.2 V க்கு இடையில் இருக்கலாம். குறைந்த சுய-வெளியேற்றம் மற்றும் அதிக எண்ணிக்கையிலான சார்ஜ்-டிஸ்சார்ஜ் சுழற்சிகள் காரணமாக, லித்தியம்-அயன் பேட்டரிகள் வீட்டு உபயோகப் பொருட்களில் மிகவும் பிரபலமாக உள்ளன.
முக்கியமான! லித்தியம்-அயன் பேட்டரிகள் அதிக சார்ஜ் செய்வதற்கு மிகவும் உணர்திறன் கொண்டவை. எனவே, அவற்றை சார்ஜ் செய்ய, அவர்களுக்காக மட்டுமே வடிவமைக்கப்பட்ட சார்ஜர்களைப் பயன்படுத்த வேண்டும், அவை அதிக சார்ஜ் செய்வதைத் தடுக்க உள்ளமைக்கப்பட்ட சிறப்பு சுற்றுகளைக் கொண்டுள்ளன. இல்லையெனில், அது பேட்டரியை அழித்து தீப்பிடிக்கும்.

நிக்கல்-காட்மியம் பேட்டரிகள் மூலம், எஃகு கட்டத்தின் மீது நிக்கல் உப்பால் கேத்தோட் ஆனது, எஃகு கட்டத்தின் மீது காட்மியம் உப்பால் ஆனோட் ஆனது, மேலும் எலக்ட்ரோலைட் என்பது லித்தியம் ஹைட்ராக்சைடு மற்றும் பொட்டாசியம் ஹைட்ராக்சைடு ஆகியவற்றின் கலவையாகும். அத்தகைய பேட்டரியின் மதிப்பிடப்பட்ட மின்னழுத்தம் 1.37 V. இது 100 முதல் 900 சார்ஜ்-டிஸ்சார்ஜ் சுழற்சிகளைத் தாங்கும்.
உதவிக்குறிப்பு! லித்தியம்-அயன் பேட்டரிகள் போலல்லாமல், Ni-Cd பேட்டரிகள் டிஸ்சார்ஜ் செய்யப்பட்ட நிலையில் சேமிக்கப்படும்.
வெப்ப இரசாயன செல்கள் காப்பு சக்தி ஆதாரங்களாக செயல்படுகின்றன. அவர்கள் சிறந்த தற்போதைய அடர்த்தி பண்புகளை கொடுக்கிறார்கள், ஆனால் ஒரு குறுகிய சேவை வாழ்க்கை (1 மணிநேரம் வரை) உள்ளது. நம்பகத்தன்மை மற்றும் குறுகிய கால செயல்பாடு தேவைப்படும் ராக்கெட் தொழில்நுட்பத்தில் அவை முக்கியமாகப் பயன்படுத்தப்படுகின்றன.
முக்கியமான! ஆரம்பத்தில், வெப்ப இரசாயன மூலங்கள் மின்சாரம் கொடுக்க முடியாது. அவர்கள் ஒரு திட நிலையில் ஒரு எலக்ட்ரோலைட்டைக் கொண்டுள்ளனர், மேலும் பேட்டரியை இயக்குவதற்கு 500-600 ° C வரை வெப்பப்படுத்த வேண்டியது அவசியம். அத்தகைய வெப்பம் ஒரு சிறப்பு பைரோடெக்னிக் கலவையால் செய்யப்படுகிறது, இது சரியான நேரத்தில் பற்றவைக்கப்படுகிறது.
உண்மையான மற்றும் சிறந்த ஆதாரத்திற்கு இடையிலான வேறுபாடு
ஒரு சிறந்த ஆதாரம், இயற்பியல் விதிகளின்படி, சுமைகளில் மின்னோட்டத்தின் நிலைத்தன்மையை உறுதிப்படுத்த எல்லையற்ற உள் எதிர்ப்பைக் கொண்டிருக்க வேண்டும். உண்மையான ஆதாரங்கள் வரையறுக்கப்பட்ட உள் எதிர்ப்பைக் கொண்டுள்ளன, அதாவது மின்னோட்டம் வெளிப்புற சுமை மற்றும் உள் எதிர்ப்பு இரண்டையும் சார்ந்துள்ளது.
சுருக்கமாக, இது நவீன மின்னோட்ட மூலங்களின் பல்வேறு வகைகளைப் பற்றியது. மேலோட்டத்தில் இருந்து பார்க்க முடிந்தால், இன்று எந்தவொரு பயன்பாட்டிற்கும் பொருத்தமான குணாதிசயங்களைக் கொண்ட பல ஆதாரங்கள் உருவாக்கப்பட்டுள்ளன.
தொடர்புடைய கட்டுரைகள்: